
东诚药业晚间公告,公司控股子公司蓝纳成收到国家药监局核准签发的关于225Ac-LNC1011注射液的药品临床试验批准通知书,同意开展前列腺癌的临床试验。该药物是一种靶向前列腺特异性膜抗原的α粒子放射性体内治疗药物,拟用于治疗PSMA阳性表达的晚期前列腺癌患者。目前国内外暂无同产品上市,亦无相关销售数据。该项目累计已投入研发费用约1453.09万元。
举报 相关阅读 中国药企出海势头不减,现在人才不够用了 | 海斌访谈
中国药企出海势头不减,现在人才不够用了 | 海斌访谈“一到出海,一到MRCT(国际多中心临床试验)之后,瞬间发现有欠缺了。”
8 397 09-20 16:48 中国澳门启动首个新药临床试验
中国澳门启动首个新药临床试验这次临床试验启动意味着粤港澳大湾区临床研究网络“最后一块拼图”得以补齐。
41 08-29 17:38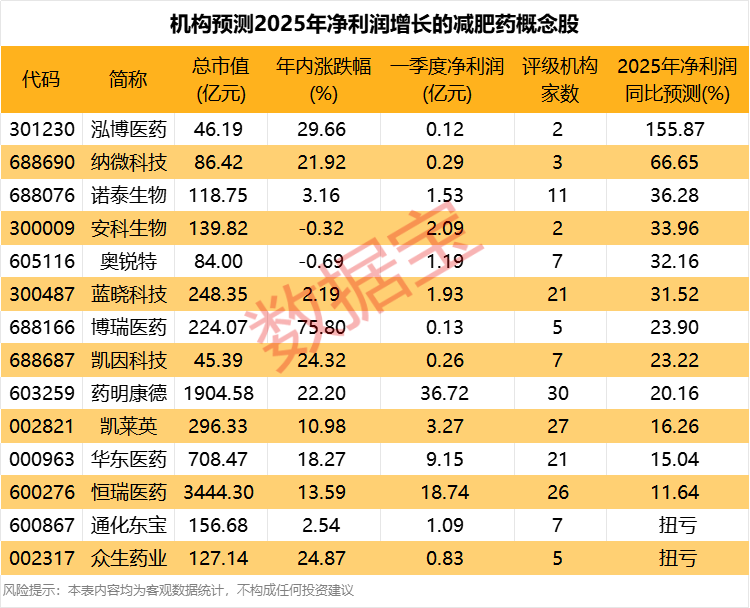 全球首个GCG/GLP-1双受体激动减重药物获批,机构预测多只减肥药概念股业绩向好
全球首个GCG/GLP-1双受体激动减重药物获批,机构预测多只减肥药概念股业绩向好全球首个GCG/GLP-1双受体激动减重药物获批,机构预测多只减肥药概念股业绩向好
27 06-27 21:23 去年我国新药临床试验数量再创新高,司美格鲁肽领跑
去年我国新药临床试验数量再创新高,司美格鲁肽领跑2024年,我国新药注册临床试验数量为近五年新高,将近5000项(4900项),较上一年增长了13.9%。
9 649 06-20 10:52 创新药临床试验审评审批提速,一类创新药等纳入30日通道
创新药临床试验审评审批提速,一类创新药等纳入30日通道此次征求意见稿,拟统一符合资质要求的药物范畴,并在“生物制品1类创新药”的基础上,还明确纳入符合要求的“中药”“化学药品”。
481 06-16 18:11 一财最热 点击关闭股票配资吧提示:文章来自网络,不代表本站观点。